A l’heure où de nombreux laboratoires semblent rivaliser en termes d’annonce quant à l’aboutissement potentiel du développement de leur vaccin contre la COVID-19, il m’a semblé intéressant de se pencher sur la nature de ces différents vaccins. Il est toujours mieux de savoir un minimum à quoi s’attendre ! 😉
J’avais déjà évoqué dans les grandes lignes le principe de la vaccination dans cet article.
Pour rappel, le principe de la vaccination repose sur la stimulation du système immunitaire adaptatif (ou spécifique), qui est doté d’une « mémoire » et fait intervenir les lymphocytes (variété de globules blancs). Dans les très grandes lignes, lorsque l’on met en contact l’organisme avec un pathogène, il va y avoir une production d’anticorps via les lymphocytes (B) (réponse primaire dans les 10 jours qui suivent le contact). Tout d’abord IgM (Immunoglobulines M), puis IgG (Immunoglobulines G produites par les lymphocytes B à mémoire). Notre système immunitaire ayant ainsi été « éduqué », lors d’un second contact avec le même pathogène, ces lymphocytes B à mémoire vont produire rapidement et en grande quantité des anticorps pour neutraliser l’agresseur avant qu’il ne puisse se multiplier. C’est la réaction dite secondaire.

On voit par exemple ci-dessus la réaction immunitaire après infection, qui implique tout d’abord la formation des anticorps IgM, qui vont finir par disparaître. Puis la formation des anticorps IgG, qui vont subsister dans le corps à long terme, et vont normalement protéger d’une 2ème infection (même si l’on doute encore de cette immunité à long terme dans le cas du Covid).
Cette formation d’IgG peut intervenir naturellement après infection par le virus, ou bien être induite par la vaccination.

De quoi est constitué un vaccin ?
Le vaccin est élaboré à partir de l’agent pathogène en question (ici virus). On distingue différentes approches :
- Les vaccins à partir de virus vivants atténués : Le virus, inactivé au moyen d’un traitement chimique qui lui fait perdre toute agressivité (d’où le terme atténué), est injecté dans l’organisme. Il va induire la production d’anticorps contre le virus en question (et aussi souvent une forme atténuée de la maladie). On utilise ici souvent des adjuvants.
- Les vaccins inactivés, qui contrairement à la forme atténuée ne déclenchent pas la maladie sous une forme fruste. Parmi eux :
- Les vaccins à base de protéine virale : Certaines protéines du virus sont isolées en laboratoire. Elles sont ensuite produites par synthèse et injectées dans l’organisme pour induire la production d’anticorps (les anticorps reconnaissant cette protéine propre au virus d’intérêt, ils vont permettre de neutraliser le virus au global si l’organisme est en contact avec le virus par la suite). C’est le cas de la protéine S, par exemple, qui est utilisée dans plusieurs des vaccins en cours de développement. Les vaccins reposant sur les protéines virales isolées ne représentent aucun risque pour l’organisme. La production de ce type de vaccin est aussi plus rapide, mais la présence d’adjuvants peut être nécessaire pour obtenir une meilleure réponse.
- Les vaccins à base d’ADN ou ARN messager plutôt que d’injecter la protéine directement, on injecte la séquence génétique qui code pour la protéine en question. A noter que l’ARN messager (simple brin) est l’intermédiaire entre l’ADN et la protéine (voir schéma ci-dessous), ou l’ARN et la protéine (le coronavirus étant par exemple un virus à ARN, à lire /relire ICI)). Une fois injecté dans l’organisme, ce code génétique est traduit en protéine via notre machinerie cellulaire, et notre système immunitaire va de la même façon réagir contre cette protéine et produire les anticorps. Ne s’agissant que d’une petite partie du code génétique du virus, il n’y a pas de caractère pathogène pour l’homme. De plus, les vaccins à ARNmessager ont l’avantage de ne présenter de risque d’intégration du matériel génétique étranger dans les cellules de l’organisme à immuniser. Contrairement aux précédents, cette technique ne nécessite a priori pas d’adjuvants.Néanmoins cette technique reste une approche nouvelle et il n’existerait a priori pas encore de vaccin commercialisé reposant sur cette technologie.
- Les vaccins à vecteur viraux : Le principe est un peu plus complexe. La séquence génétique d’intérêt est acheminée à nos cellules via un vecteur viral, autrement dit un virus (autre que le covid ici), mais qui a été modifié pour ne pas être pathogène. Ce vecteur viral va en gros servir uniquement de transporteur (c’est aussi le principe utilisé dans les thérapies géniques par exemple). L’avantage est que cela pourrait être plus efficace, mais les inconvénients sont qu’il faut produire le vecteur en question en amont, et que ce vecteur viral peut ne pas être neutre une fois injecté à l’organisme et interférer avec le système immunitaire. Le leader dans cette technologie est le groupe Johnson & Johnson (dont Janssen est une filiale).

Le processus de développement d’un nouveau médicament / vaccin
Rappelons également dans les grandes lignes comment se passe le développement d’un nouveau médicament (ou vaccin). Avant de pouvoir être commercialisé, celui-ci devra bénéficier d’une AMM (Autorisation de Mise sur le Marché) signifiant que son efficacité ET sa sécurité auront été éprouvées selon des processus bien définis. L’AMM est délivrée par les autorités nationales compétentes (comme l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) en France, ou par l’Agence européenne des médicaments (EMA) dans les cas de procédures centralisées en Europe, ou bien auprès de la FDA (Food and Drug Administration) aux Etats-Unis. Ceci pose d’ailleurs la question des zones hors Europe et Etats-Unis (je ne m’étais jamais vraiment posée la question à vrai dire, si toutefois certains d’entre vous savez quelles sont les règles pour un laboratoire chinois par exemple qui souhaiterait lancer son médicament sur le marché chinois ?)
Pour obtenir cette AMM, le chemin est long (et bien balisé).
L’étude pré-clinique, réalisée chez l’animal : une fois la molécule / le médicament développé, cette première étape permet d’acquérir les premières connaissances sur la molécule ou le futur vaccin – pharmacologie (mécanisme d’action, activité), pharmacocinétique (comportement et devenir dans l’organisme) et toxicologie (toxicité) – avant de débuter les études chez l’homme.
Puis vient l’étude clinique à proprement parler (réalisée chez l’homme). Elle est divisée en 4 phases, dont 3 jusqu’à l’AMM :
Phase I : Cette phase est menée sur un petit groupe de volontaires. Selon le médicament ou la molécule concernée, les volontaires seront sains ou malades. L’objectif est ici d’étudier la cinétique de la molécule (son devenir dans l’organisme après administration, sa rapidité d’élimination, les différents métabolites produits, etc.), son seuil de tolérance, les effets indésirables, ainsi que sa toxicité. Si les résultats sont encourageants, on passe alors à l’étape suivante.
Phase II : Elle a lieu chez des volontaires malades et va avoir pour objectif d’évaluer l’efficacité de la molécule, et de déterminer la dose optimale (la posologie). Cette phase est généralement menée contre placebo (un groupe reçoit un substitut sans activité, alors que le second groupe reçoit la molécule testée), ce qui permet comparativement d’évaluer l’efficacité. Ni les patients, ni les médecins ou investigateurs ne savent quels sujets reçoivent le traitement versus le placebo (on parle de double aveugle, donc au final « double aveugle contre placebo », vous verrez souvent ce terme). Cette approche permet d’éliminer tout biais dans l’étude. L’aveugle ne sera levé qu’une fois l’essai achevé. Si les résultats sont probants, on engage alors la phase III.
Phase III : Cet essai est réalisé sur un panel de sujet plus vaste (plusieurs centaines, idéalement plusieurs milliers de volontaires, et si possible de différentes zones géographiques (selon nos origines, nous n’avons pas tous le même métabolisme, ni le même environnement !). Lorsque vous entendez parler d’étude multicentrique, cela signifie qu’elle implique plusieurs centres investigateurs (hôpitaux ou autres). L’efficacité de la molécule va être comparée au traitement de référence (s’il existe), ou au placebo. Ici encore, le double aveugle est généralement pratiqué pour éviter les biais. Cette phase permet aussi d’enrichir les connaissances sur la molécule en question (confirmer les doses efficaces, identifier plus largement les effets indésirables sur une population bien plus vaste, évaluer le bénéfice / risque…). Ces essais de phase III peuvent durer des années.
Si les résultats sont positifs à l’issue de cette phase III, on demande enfin l’AMM auprès des autorités compétentes pour pouvoir le commercialiser.
Mais l’étude ne s’arrête pas là, il existe encore une phase, la phase IV, qui est une étude à long terme. Il s’agit d’une phase épidémiologique où l’on va observer et recenser, après la commercialisation, les éventuels effets indésirables rares qui pourraient survenir chez les personnes à qui la molécule /le médicament a été administré, ou bien les interactions médicamenteuses, etc… (phase de pharmacovigilance, par l’intermédiaire de systèmes de notification aux autorités de santé) (si un jour par exemple, vous faites une réaction anormale à une certaine substance, votre médecin peut (ou même devrait) le signaler aux autorités de santé, ce qui permet d’enrichir les données).
Pour les vaccins, le process va être grosso modo le même. Si ce n’est que la phase II peut-être divisée divisée en deux.
La phase IIA (qui peut durer 1 à 2 ans), sur un petit nombre de volontaires, va permettre de continuer à évaluer la tolérance et la sécurité du vaccin potentiel. Elle permet également d’étudier son immunogénicité (sa capacité à stimuler la production d’anticorps dans l’organisme), et de définir la dose optimale de vaccin.
La phase IIB (preuve de concept) dure en moyenne de 2 à 5 ans. L’objectif est :
- De déterminer si le vaccin permet bien une protection durable contre l’infection
- De définir la stratégie vaccinale (dose, nombre de rappels), etc.
Suivra alors l’essai de phase III si les résultats étaient probants (mesure de l’efficacité et bénéfices / risques), qui peut également durer de 3 à 5 ans.
Lorsque l’on voit la durée moyenne de ces différentes phases d’étude, on mesure combien le développement de l’actuel vaccin contre le covid-19 a été une course contre la montre.

Une course à l’échelle mondiale
De nombreux laboratoires (près d’une cinquantaine à priori) se sont engagés dans le développement d’un vaccin contre le SARS-CoV 2. Cinq d’entre eux étaient récemment en cours d’essais cliniques de phase III de grande taille (plus de 10 000 sujets). D’autres sont en cours sur des panels plus modestes. L’ensemble représentant plus de 200 000 sujets inclus à travers le monde.
Selon les laboratoires, les vaccins en cours de développement reposent sur des principes différents : virus inactivés, recombinants, vectorisés sans réplication (au sein d’adénovirus humains ou de singe) et à ARN messager (ARNm) (pour rappel, le coronavirus est un virus à ARN, à relire cet article). D’autres vaccins sont à des stades plus précoces d’avancement : virus vivants atténués (administrés par voie intranasale), vectorisés avec réplication (au sein de virus Influenza ou de virus des oreillons), à ARN autoréplicant ou à ADN. Tout ceci peut paraître un peu compliqué, mais je vais essayer d’expliquer un peu plus clairement sur quels principes reposent les vaccins actuellement au stade le plus avancé de développement (je n’aborderai pas les laboratoires chinois, pourtant nombreux à travailler sur le sujet).
Moderna Therapeutics : Cette société américaine dirigée par un français (mRNA-1273) a développé en collaboration avec l’Université de Cambridge un vaccin à base d’ARN messager (matériel génétique du virus) codant pour l’une des protéines du virus (Protéine Spike (S), qui est la clé qui permet à ce virus de pénétrer dans nos cellules). Le vaccin nécessite deux injections (dose de 100 µg par injection).
Il est en cours de phase III et a été testé sur plus de 30.000 personnes au total aux Etats-Unis (Etude COVE). Le 16 novembre, Moderna a annoncé des résultats intermédiaires d’analyses. 95 cas de covid ont été recensés parmi les sujets testés, parmi lesquels 90 cas dans le groupe placebo, versus 5 dans le groupe ayant reçu le vaccin, ce qui représente une efficacité de 94,5%. Cette efficacité a été évaluée 2 semaines après l’administration de la seconde dose de vaccin.
L’étude intermédiaire s’est aussi penchée sur 11 cas sévères de COVID recensés. Les 11 étaient présents dans le groupe placebo et aucun dans le groupe vaccin.
En termes de sécurité, aucun trouble grave n’a été observé suite à l’administration du vaccin, mais certains effets secondaires ont été recensés : fatigue (9,7%), douleurs musculaires (8,9%), douleurs articulaires (5,2%), maux de tête (4,5%), douleur (4,1%).
Le communiqué de presse complet est disponible ici.
La société envisage de soumettre dans les prochaines semaines une Autorisation d’Usage d’urgence (Emergency Use Auhtorization) auprès de la FDA, sur la base d’un essai un peu plus vaste sur 151 cas et un suivi de 2 mois. Les Etats-Unis ont déjà passé un accord à la hauteur de 1,525 milliards de dollars pour se procurer ce vaccin.
Le vaccin peut a priori se conserver 30 jours entre 2 et 8° C (soit la température du frigo), ce qui parait bien plus gérable en termes de logistique que le vaccin de Pfizer qui doit être conservé à -80°C (soit une température bien plus basse que celle d’un congélateur classique).
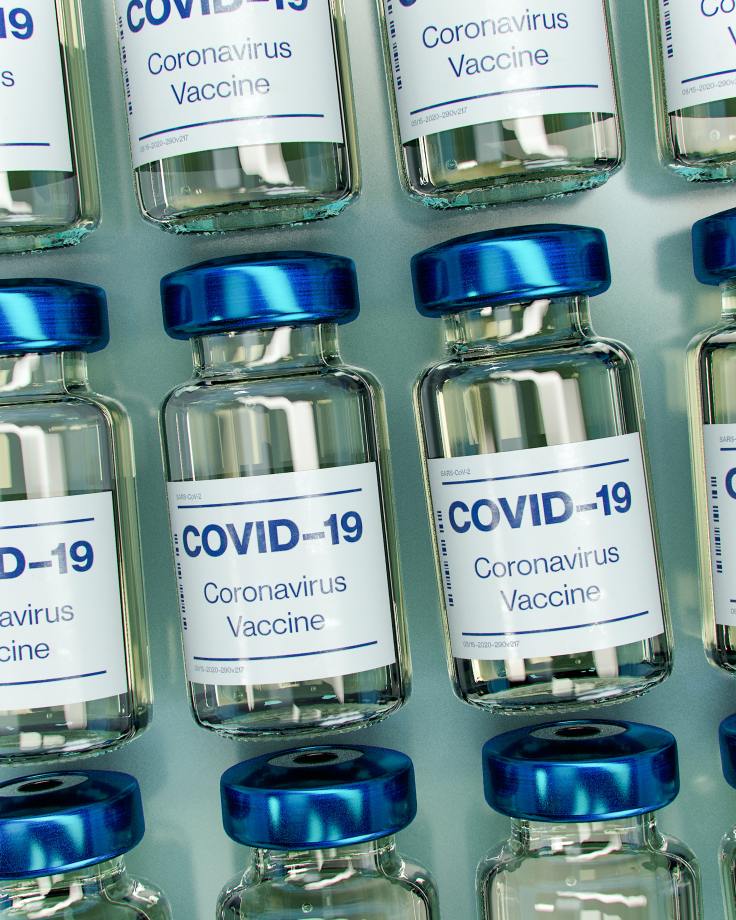
Le vaccin développé par le laboratoire américain Pfizer, associé à la biotech allemande BioNTech (BNT162b2), repose sur le même principe d’ARN messager (modifié ici), codant de même pour la protéine Spike. Leur étude de phase III porte quant à elle sur 43 500 sujets. L’efficacité a été estimée le 9 novembre à 90% (7 jours après la 2nde dose et 28 jours après la 1ère injection), sur 94 sujets ont déclaré le COVID répartis entre le groupe placebo versus vaccin. L’efficacité a ensuite été portée à 95% le 18 novembre, estimée sur 170 cas confirmés (162 dans le groupe placebo et 9 dans le groupe vaccin).
Le communiqué de presse est ici.
Il y a 48 heures, Pfizer a annoncé avoir demandé une autorisation d’utilisation d’urgence auprès de la FDA, et a engagé la démarche dans beaucoup d’autres pays à travers le monde (Australie, Canada, Europe, Japon et UK).
Astrazeneca, groupe pharmaceutique né de la fusion (1999) du suédois Astra et de l’anglais Zeneca, a travaillé en collaboration avec l’Université d’Oxford, pour développer un vaccin reposant sur un principe différent (pour schématiser, un vecteur qui va permettre dans l’organisme la production de la protéine S citée précédemment, contre laquelle les anticorps vont être produits, cas du « vaccin à vecteur viral » mentionné précédemment).
Pour aller plus loin :
Le vecteur est ici une version affaiblie d’un virus du rhume commun (adénovirus) qui provoque des infections chez les chimpanzés, dans lequel a été introduite la séquence génétique de la protéine Spike (S), toujours elle, du coronavirus SRAS-CoV-2. Après vaccination, la protéine Spike sera de même produite dans l’organisme humain, induisant une réaction du système immunitaire.
Leur stade d’avancement est un peu moins poussé. Les résultats de l’étude de phase II (560 participants) ont été publiés récemment dans la revue The Lancet (l’étude ici). Le protocole est ici un peu plus compliqué, mais cette étude a montré que le vaccin induit chez les sujets plus âgés (plus de 56 ans, potentiellement plus à risque) une réponse immunitaire identique à celle induite chez les plus jeunes (18 à 55 ans).
Début septembre, Astrazeneca avait annoncé une pause de ses essais cliniques après « une maladie potentiellement inexpliquée » chez un sujet de l’étude (inflammation de la moelle épinière), dans le doute qu’il s’agisse d’un effet secondaire grave. L’essai a ensuite été repris un peu plus tard avec l’accord des autorités sanitaires britanniques.
Janssen : Leur vaccin repose sur une technologie mise au point il y a une dizaine d’années, à base d’un adénovirus (Adénovirus 26 humain) (vecteur viral non réplicatif, c’est-à-dire qu’il ne se multiplie pas), porteur de la protéine S. L’étude clinique de phase III a été lancée le 23 septembre, avec le début de recrutement de 60 000 sujets aux Etats-Unis et en Europe. L’essai a été suspendu temporairement mi-octobre après « une maladie inexpliquée » chez un participant de l’étude. Je n’ai pas trouvé d’information indiquant que l’étude avait repris.
La vaccination repose sur l’injection d’une seule dose, ou de deux doses (J0 et J56) (l’essai sur 60 000 personnes est prévu avec une seule dose).
Novavax : ce laboratoire américain a également recours à une technologie plus complexe. Leur vaccin a été développé en utilisant une technologie à base de nanoparticules (particules de taille infime), qui contiennent des fragments de la protéine S, avec l’un de leur adjuvant breveté (Matrix M), pour augmenter la réponse immunitaire.
La protéine S est ici recombinante, c’est-à-dire que la séquence génétique codant pour la protéine S du SARS CoV 2 a été combinée au matériel génétique d’un baculovirus (un virus qui infecte les insectes). Ci-dessous la représentation d’un (ici ADN) recombinant.

Ce matériel génétique de baculovirus modifié (incluant donc la séquence de la protéine S) a été exprimé / traduit dans des cellules d’insectes (la cible originelle de ce baculovirus), ce qui a permis de produire la protéine S (ensuite purifiée et associée aux nanoparticules du vaccin). (bon ceci, c’est si j’ai tout bien compris, pour la version chinoise, c’est ici). 😉
Enfin, petit dernier, le français Sanofi, qui travaille en collaboration avec le laboratoire britannique GSK. Leur étude estencore en phase I-II (sur 440 sujets). Le principe repose également sur l’usage d’une protéine recombinante, technologie déjà utilisée pour le vaccin contre la grippe (pas de détails supplémentaires sur la constitution du vaccin). De même que pour Novavax, un adjuvant est utilisé. Leur objectif est d’obtenir les premiers résultats en décembre, avant d’enclencher la phase III. SI les résultats de cette dernière sont probants, une demande d’approbation réglementaire pourrait être soumise au premier semestre 2021.
A noter que Sanofi travaille également sur une 2ème stratégie en collaboration avec Translate Bio, avec un vaccin à base d’ARN messager.
En conclusion…
Tout ceci souligne que le sujet est bien complexe, l’objectif étant de trouver un compromis entre un vaccin suffisamment efficace tout en déclenchant le minimum d’effets secondaires indésirables (vu les délais de développement, on prend ici peu de recul quant à la survenue de ces effets secondaires potentiels…). Et ce vaccin devra idéalement ne pas être trop compliqué à produire (pour pouvoir répondre à une très forte demande sous des délais très courts) tout en permettant une logistique réaliste (avec un vaccin devant être conservé à -80°C par exemple, cela impliquerait la vaccination dans des centres très spécifiques, excluant la possibilité de vaccination en cabinet ou même à la maison).
On a vu que les mesures prises jusqu’alors en Europe et ailleurs (gestes barrière, confinement, couvre-feu, mesures intermédiaires), ne suffisent pas à stopper et bien difficilement à ralentir l’épidémie (et quoique beaucoup en disent, oui, sans mesures, c’est bien pire). Un confinement très strict, comme cela a été le cas en Chine, a visiblement permis de se débarrasser quasi totalement du virus (aaaah les bonnes dictatures ! 😉 cependant une telle approche ici aurait tout simplement été inimaginable (déjà que certains montent au créneau lorsqu’on leur demande de porter le masque !) (bon ceci dit, les chiffres de la Chine restent toujours sujets à caution, lorsque l’on sait leur politique de communication). De plus, vu les échanges et les déplacements très importants à l’échelle mondiale au 21ème siècle, pour que ces mesures seules soient efficaces, il faudrait que TOUTES les zones où il existe des cas appliquent ces règles. Ce qui est encore moins concevable.
C’est pourquoi l’un des espoirs pour sortir rapidement de cette situation était la vaccination.
Cependant, l’intérêt de ce vaccin dans la stratégie de contrôle de l’épidémie dépendra également du taux de population acceptant de se faire vacciner (imaginons que seule une faible partie de la population se fasse vacciner, cette faible proportion sera elle protégée, mais cela ne suffira pas à endiguer l’épidémie, car la majorité de population non vaccinée continuera à véhiculer le virus).
Quant à savoir quelles populations seront prioritaires ? personnel soignant sans doute (je ne suis pas certaine néanmoins que cela puisse leur être légalement imposé ?), personnes âgées en EHPAD (s’agissant de personnes potentiellement plus fragiles, on peut aussi se demander si le risque n’est pas accru d’administrer des vaccins sur lesquels on aura encore peu de recul ?)
Est-ce que la solution serait finalement de vacciner les plus jeunes (15-40 ans) qui semblent davantage vecteurs ?
Il n’y a malheureusement pas de réponse claire à tout cela.
A lire également cet article :
et cette infographie très bien faite

De quand datent ces informations très formatées, qui ne tiennent absolument pas compte des effets désastreux et trop nombreux pour qu’on puisse ne pas remettre en question des injections géniques étudiées à la hâte ‘bien que vingt années de recherche sur les SARS les aient anticipées ?
Jamais lu de telles inepties sur un site de naturopathe ! Pour les bienfaits du vaccin de la variole, l’histoire n’est pas celle qu’on colporte comme un dogme (en train de s’effondrer).
Bonne chance à vous pour la suite de votre parcours vaxx. si vous n’ouvrez pas vos yeux.
J’aimeJ’aime
Bonjour, comme cela est indiqué sous l’article, il a été publié en novembre 2020.
Avant d’être naturopathe, je suis avant tout scientifique et me base sur des informations croisées et étayées. Ce qui est navrant d’ailleurs chez bon nombre de naturopathes, c’est de relayer des informations sorties du chapeau, parfois même non comprises.
Pour ce qui est des « effets désastreux » dont vous parlez, à quel vaccin faites-vous allusion ? car ils reposent sur des principes très différents, et leurs effets secondaires potentiels (qui existent, oui, comme pour tout autre médicament) sont très différents. N’hésitez pas à partager vos sources.
De même pour ce « dogme » de la variole, là aussi vos sources sont les bienvenues !
J’aimeJ’aime